
粤港澳中枢神经再生研究院闫森、李晓江教授团队在Nature Biomedical Engineering发表小胶质细胞-T细胞相互作用驱动亨廷顿病神经变性相关成果
暨南大学融媒体中心讯 近日,暨南大学粤港澳中枢神经再生研究院闫森、李晓江教授团队在生物医学领域顶级期刊Nature Biomedical Engineering(IF = 26.7)上发表标题为“Single-nucleus transcriptomics of an engineered pig model reveals microglia-T cell interactions driving Huntington’s disease neurodegeneration”的研究成果。粤港澳中枢神经再生研究院闫森研究员、李晓江教授为共同通讯作者。李嘉威博士(现暨南大学附属广州红十字会医院博士后)和林颖琪博士研究生为共同第一作者。

论文截图
亨廷顿病(Huntington’s disease,HD)是一种致命的神经退行性疾病,其病因源于亨廷顿基因(Huntingtin,HTT)1号外显子中CAG三核苷酸重复序列的异常扩增。近年来,研究发现包括阿尔茨海默病(Alzheimer’s disease,AD)与帕金森病(Parkinson disease,PD)在内的多种神经退行性疾病中均存在大脑内T细胞浸润现象,且该现象与神经退行性病变进程密切相关。然而,在HD中是否发生类似的T细胞浸润及其在疾病进展中的具体作用仍不清楚。为探究此问题,本研究利用课题组前期构建的能够精准模拟HD患者纹状体选择性神经退行性病变的HD基因敲入(HD-KI)猪模型,并结合多种HD啮齿类模型及人类HD患者单细胞数据,开展跨物种比较分析。通过单细胞转录组测序分析,我们成功构建了国际上首个HD-KI猪纹状体的单细胞图谱。跨物种单细胞图谱分析显示,猪纹状体在细胞组成与比例方面与人类高度相似,这一发现进一步确立了猪模型相较于传统啮齿类模型在模拟亨廷顿病复杂病理方面的独特优势。
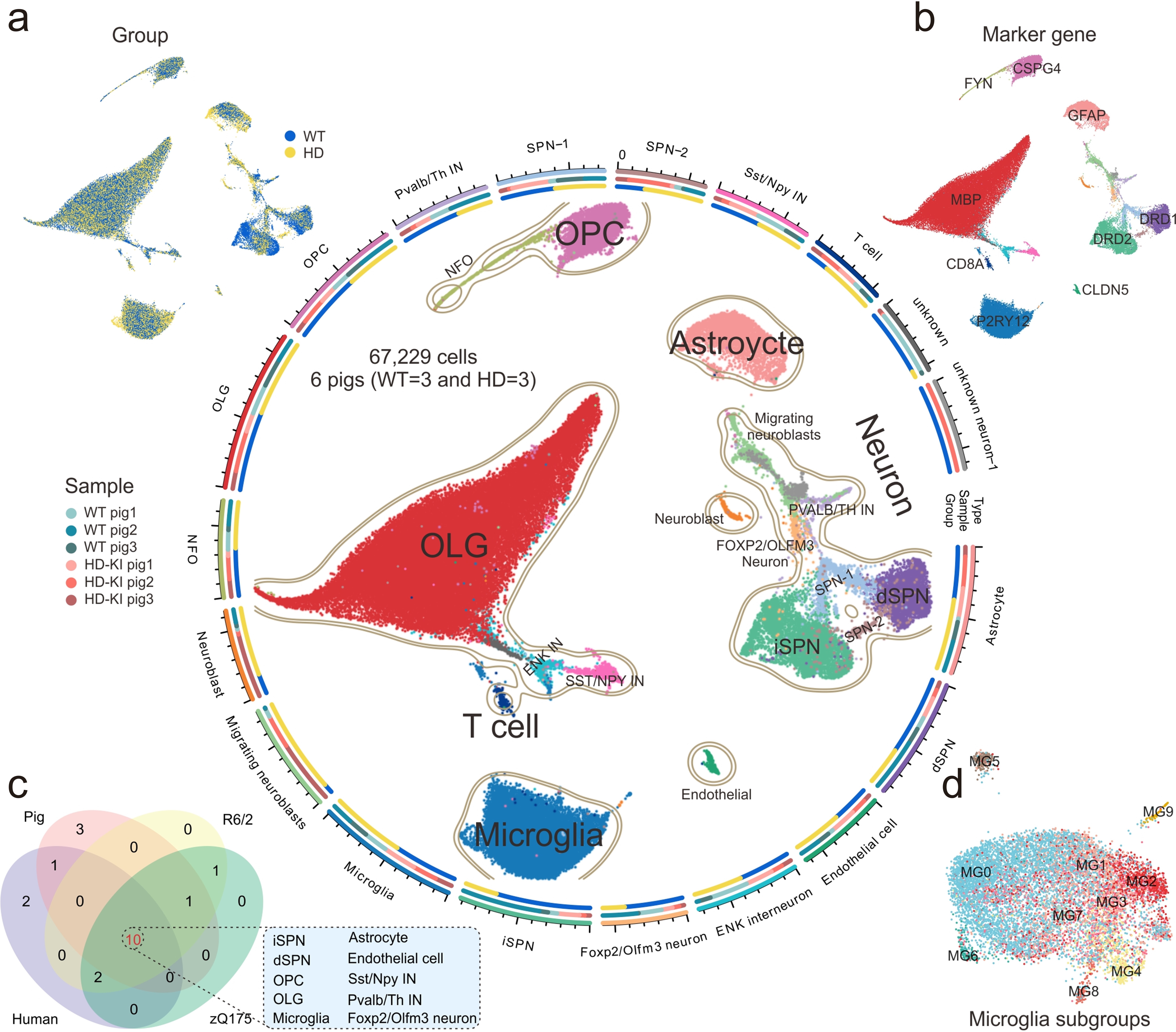
WT/HD-KI猪纹状体单细胞图谱
HD-KI猪模型准确再现了HD患者中典型的纹状体中型多棘神经元选择性丢失,而该病理特征在HD-KI小鼠中不明显。更重要的是,本研究首次在HD患者及HD-KI猪的纹状体中共同发现CD8⁺ T细胞的浸润,而HD小鼠模型缺乏该病理现象。
机制研究表明,浸润的CD8⁺ T细胞表达CCR5受体,并通过CCL8-CCR5趋化轴被招募至病变纹状体区域,该过程由HD中激活的IFITM3⁺小胶质细胞亚群分泌的CCL8趋化因子所介导。浸润的CD8+T细胞在纹状体中通过释放穿孔素和颗粒酶诱导神经元变性,从而加剧HD神经退行性病变。尽管在HD-KI小鼠中未观察到内源性CCL8上调和CD8+T细胞浸润,外源性CCL8过表达却足以在其纹状体中诱发CD8⁺ T细胞浸润并发生神经元丢失,提示物种特异性小胶质细胞反应可能调控T细胞的中枢浸润。
进一步干预实验表明,使用CCL8中和抗体可有效阻断CD8⁺ T细胞的纹状体浸润并缓解神经元变性。这些发现不仅揭示了小胶质细胞与T细胞的互作在HD神经免疫机制中的核心作用,也为理解适应性免疫在疾病进展中的功能及开发相应干预策略提供了关键理论依据。
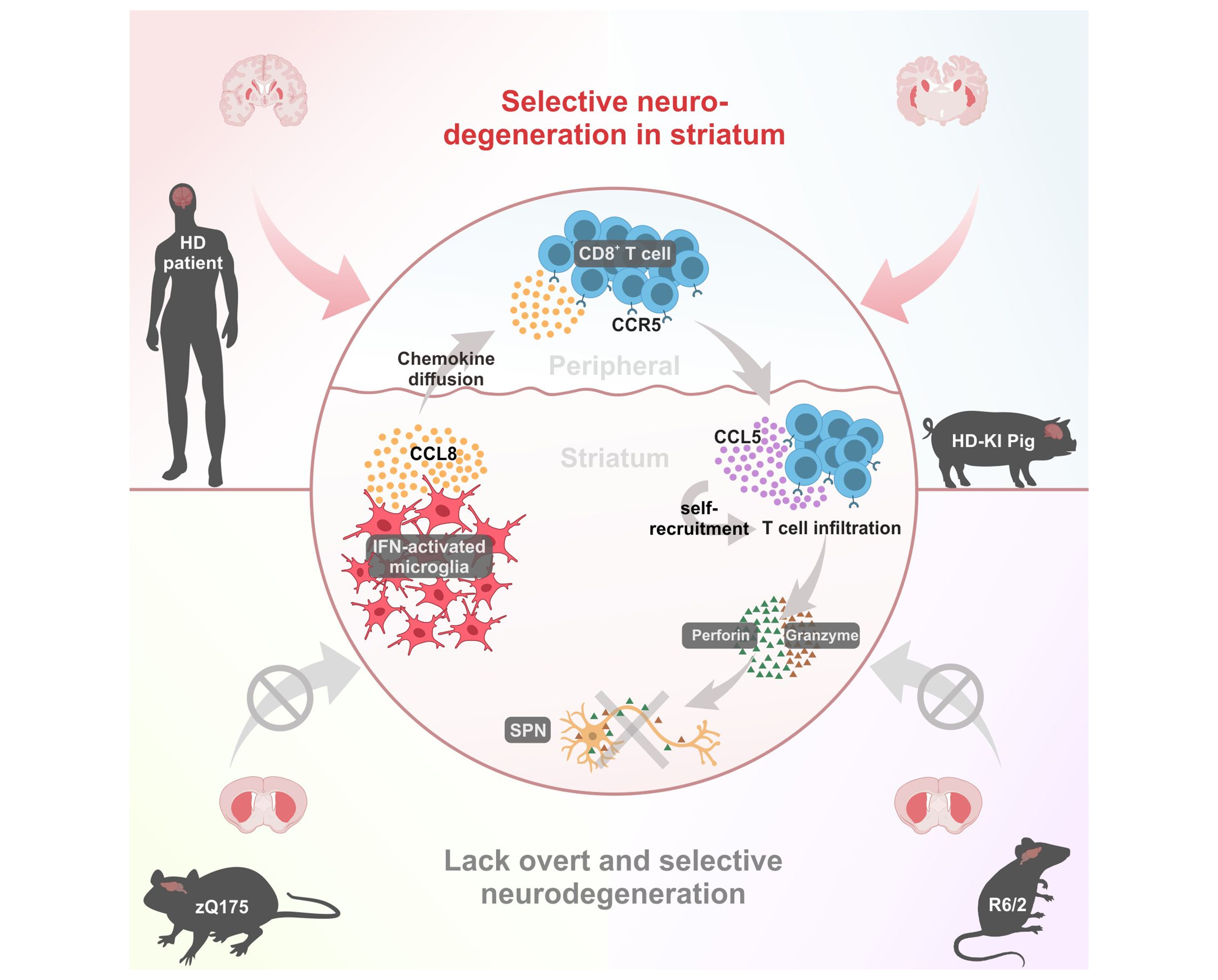
CD8+T细胞驱动HD神经退行性变的示意图
本研究受到国家重点研发计划、国家自然科学基金委、广州市脑科学重点研究计划、广东省科技厅、广州市科技局、暨南大学、广东省非人灵长类动物模型研究重点实验室、暨南大学生物活性分子与成药性优化全国重点实验室和暨南大学王宽诚基金会的大力支持。
论文链接:https://www.nature.com/articles/s41551-026-01621-x
责编:苏倩怡




